概要

漫画Dr.STONEで鍵となるのは、何と言っても石化を解除できる"復活液"です。
復活液のレシピが硝酸とアルコールの混合液であることは、物語の初期段階で判明していました。

しかし、硝酸に関してはコウモリの糞からわずかに取れるのみで、十分な量を確保できていませんでした。作中では少ない復活液やそのレシピを巡って、主人公の"石神千空"と霊長類最強の高校生"獅子王司"が争っていました。

そんな硝酸の供給事情が変わったのは、石化王国編で白金(プラチナ)を入手したときです。
白金を触媒としてアンモニア酸化法で硝酸を人工的に生産することができるようになったのです。
このアンモニア酸化法は1902年にOstwaldによって開発された代表的な工業的製法です。
この記事では、アンモニア酸化法がどのようなプロセスとなっているか解説します。
アンモニア酸化法
作中での製造装置

作中では上のような装置で硝酸を製造していました。
漫画とは思えないくらいアンモニア酸化法のプロセスをよく表現できています。
ただ細かいことを言うと、1000℃弱の高温と高圧に耐えられる装置なのかは少々疑問が残ります。
もちろん漫画なので現実を再現する必要は全くなく、読者にわかりやすいように省略・デフォルメ化しているのだと思います。
アンモニア発生装置

作中では尿からアンモニアを作っていますね。
作中で解説がないため正確なことはわかりませんが、おそらく尿素の分解反応でアンモニアを生成しているのだと思います。
$$NH_{2}CONH_{2}⇔HNCO+NH_{3}・・・(1)$$
$$HNCO+H_{2}O⇔CO_{2}+NH_{3}・・・(2)$$
(1)、(2)式のように、理想的には1molの尿素から2molのアンモニアを得ることができます。
ただし実際には反応速度が遅く、現実的な生産能力を確保しようとすると、触媒や酵素が必要となります。

作中では後にハーバーボッシュ法によるアンモニア合成法が登場するため、尿素分解によるアンモニア生成法はストーリー的にあまり深掘りしなかったのかもしれません。
アンモニア予熱器

常温のアンモニアをそのまま反応器に供給するのは効率が悪いので予熱して温度を上げます。
円板状の予熱器が設置されているのがわかりますね。
酸素供給ライン
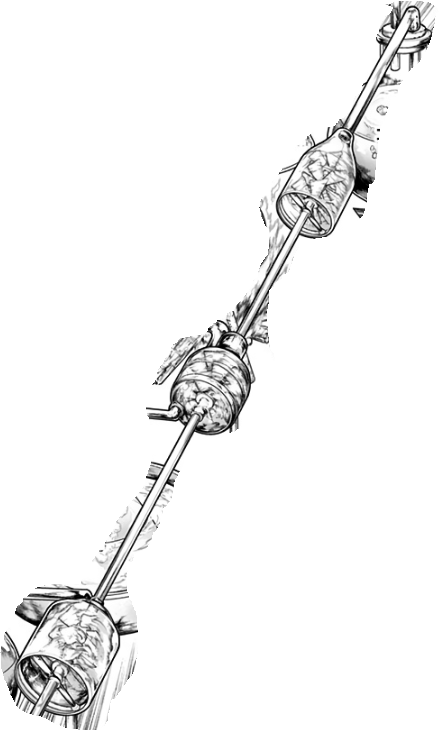
アンモニアの酸化には酸素が必要で、空気中の酸素を使用することが多いです。
風車のような装置で空気をアンモニア水に送り込んでいるのがわかります。
アンモニア酸化器

原料のアンモニアを酸化して一酸化窒素(NO)を生成します。
$$4NH_{3}+5O_{2}⇔4NO+6H_{2}O・・・(3)$$
この(3)式の反応に白金触媒が必要なため、主人公達は白金を探していたわけですね。
ものすごい発熱反応で、工業的には700~1000℃で運転しています。
一酸化窒素冷却器
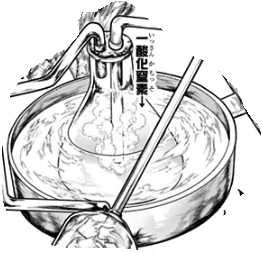
(3)式で生成した一酸化窒素(NO)をさらに酸化し二酸化窒素(NO2)を生成します。
$$2NO+O_{2}⇔2NO_{2}・・・(4)$$
(4)式は温度が低いほど正方向の反応速度が速くなる特徴を持っているため、反応ガスを冷却する必要があります。
作中の画像を見ると、たらいに水か何かの液体を入れて三角フラスコを冷却しています。
二酸化窒素吸収器
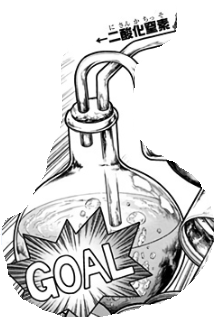
(4)式で生成した二酸化窒素(NO2)を水に吸収させて硝酸を得ます。
$$3NO_{2}+H_{2}O⇔2HNO_{3}+NO・・・(5)$$
作中の画像をだと、丸底フラスコに入れた水に二酸化窒素を吹き込ませて吸収させていますね。
以上のように、漫画では各反応の特徴を捉えてちゃんと描写していることがわかります。
では、実際の製造装置ではどうなっているのでしょうか?
工業的な製造装置
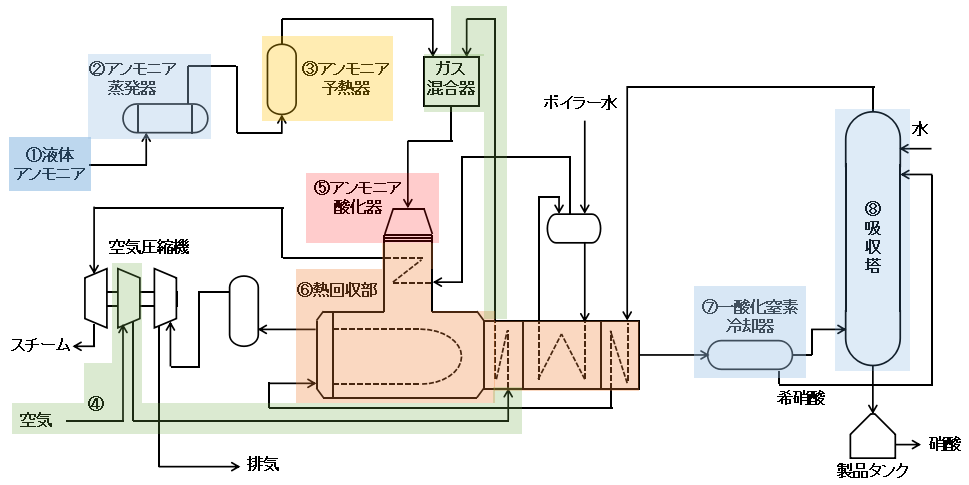
上図にアンモニア酸化法の製造プロセスの概要を示します。
細かく説明するときりがないので、主要な機器のみ載せています。
実際の製造装置でもプロセスの考え方は変わりませんが、経済性や効率を重視したものとなっています。
①アンモニア調達

原料となるアンモニアは他社から購入するか、アンモニア製造プラントがあれば自社生産したものを使用します。
アンモニア合成は前述したハーバーボッシュ法をベースとしたプロセスが最も一般的です。
別途記事にするかもしれません。
②アンモニア蒸発器
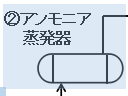
液体のアンモニアを加熱して蒸発させています。
加熱といってもアンモニアの沸点は-33℃であるため、減圧して常温の冷却水と熱交換させるだけで蒸発します。
装置は横型のケトル式蒸発器を使用することが多いようです。
縦型の蒸発器でもアンモニアを加熱蒸発させることはできます。
しかし蒸発器の断面積が小さいとアンモニアの液滴が蒸気に同伴するエントレインメントが起こりやすく、後工程の反応を考えると横型の方がよいでしょう。
③アンモニア予熱器
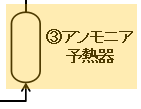
蒸発させたアンモニアをさらに加熱してアンモニアの過熱蒸気を作ります。
蒸発させたアンモニア蒸気は沸点に近いガスなので、このアンモニア予熱器がないと酸化反応器にたどり着く前に配管等の熱損失でアンモニア蒸気が一部凝縮してしまう可能性があります。
このような気液混相状態で反応工程に送ってしまうと、反応器内で濃度ムラや温度ムラが生じて一酸化窒素(NO)の収率が下がります。
したがって、多少の熱損失では凝縮しない温度まであらかじめ昇温しておきます。
④空気供給ライン~ガス混合器
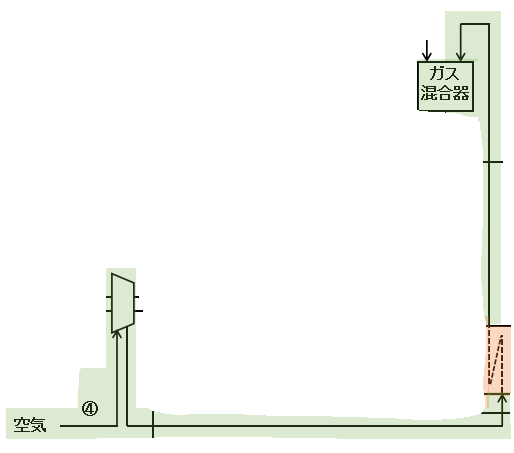
工業的な酸化反応は空気中の酸素を使うことがほとんどです。
空気圧縮機で昇圧して供給し、アンモニアと混合させます。
ただ、別途熱源を設置するとその分コストがかかりますので、アンモニア酸化後の高温のプロセスガスと接触させることで熱回収しつつ空気を予熱します。
⑤アンモニア酸化器

(3)式のアンモニア酸化反応を行なう反応器です。
金網状に加工された触媒層にアンモニアと空気の混合ガスを接触させて反応させます。
作中では白金触媒を使用していましたが、実際には白金にロジウムを5~10%加えた白金-ロジウム触媒を使用することが多いです。
(3)式の反応は通常、90%以上の一酸化窒素(NO)収率が得られます。
⑥熱回収部
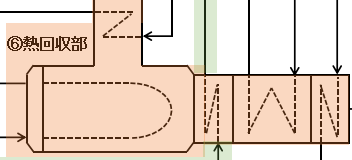
アンモニア酸化後の反応ガスは700~1000℃の高温であるため、熱源として優秀です。
(4)式の反応を行なうためには140℃程度まで冷却する必要がありますが、作中のように単に水で冷却すると熱を捨てていることになり、せっかくの熱源がもったいないです。
なるべく熱回収して有効利用できるように設計されています。
このプロセスでは
・スチーム過熱器
・排ガス加熱器×2
・空気加熱器
・ボイラー水加熱器
5つの熱交換器で熱回収しています。
上の概要図ではアンモニア酸化器と5つの熱交換器が一体の装置となっていますが、別々の機器に分かれている場合もあります。
熱回収された一酸化窒素(NO)を含むガスは温度がどんどん下がり、その過程で(4)式の反応により二酸化窒素(NO2)へ変化します。
⑦一酸化窒素冷却器
この装置でプロセスガスを最終的に常温付近まで冷却し、(4)式の反応を完了させます。
プロセスガス中に微量に含まれる水はこの冷却器で凝縮してガスと分離します。
分離した水には二酸化窒素(NO2)が溶けて希硝酸となっているため、後段の吸収塔に供給して利用します。
⑧二酸化窒素吸収塔

二酸化窒素を含むプロセスガスを下に供給し、上から水を供給することで二酸化窒素が水に吸収され、(5)式の反応が起こります。
いかに効率よく水とガスを接触させるかがポイントになります。
作中ではフラスコに入れた水中にガスを吹き込んでいますが、ガスの吹込み回数が1回だけだと二酸化窒素が吸収しきれずロスする可能性があります。
なるべく複数回ガスと液が接触するようにして吸収効率を上げるべきです。
実際には不規則充填物を詰めた充填塔や棚段塔を使用し、効率よくガスを吸収しています。
吸収塔の塔底の出口では濃度約68%の硝酸が得られます。
まとめ
漫画Dr.STONEで登場した硝酸の工業的製法について紹介しました。
アンモニアを酸化させることで硝酸を製造しています。
たった1つの物質を作るために様々な苦労や工夫があることが、作中からもよくわかりますね。
ストーリーも非常に面白いので、ぜひ読んでみてはいかかでしょうか。
