概要
Txy線図、Pxy線図のような線図上において、沸点曲線と露点曲線を平行に繋いだ線をタイラインといい、この線上で物質収支が成り立つ関係のことをてこの原理といいます。
最もよくイメージされやすいのはTxy線図上での、てこの原理です。
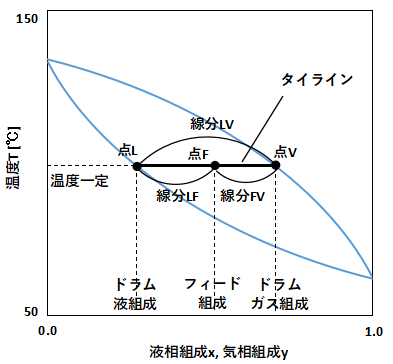
上のグラフにTxy線図とタイラインを示します。
このグラフの関係は下図のようなドラムに流体をフィードし、出口液と出口ガスにどのような組成で分かれるかを意味しています。
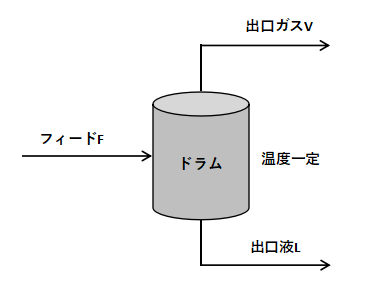
仮に、温度、圧力、組成がグラフの点Fの状態の流体をフィードします。
点Fは沸点曲線と露点曲線の間にあるため、気液混相状態にあります。
ここでドラムの温度をフィード温度と同じになるよう一定に保った場合、ドラムの中で気液は分離しタイライン上を動きます。
その結果、ドラムの下からは点Lの組成の液が出ていき、上からは点Vの組成のガスが出ていきます。
したがって、分離後の成分組成は沸点曲線及び露点曲線とタイラインとの交点である点L、点Vの値を読み取ればわかります。
加えて、物質収支はタイラインの線分の長さの比から算出することができます。
$$V=\frac{LF}{LV}F・・・(1)$$
$$L=\frac{FV}{LV}F・・・(2)$$
V:気相モル流量、L:液相モル流量
F:フィードモル流量
LF:線分LFの長さ、FV:線分FVの長さ
LV:線分LVの長さ
気相モル流量V、液相モル流量Lは(1)、(2)式から算出できます。
もちろん、真面目に系全体の物質収支と各成分の物質収支について式を立てれば、同じ値を算出することはできます。
しかし、てこの原理は作図で簡便に各成分の組成やモル量を求めることができるので、化工シミュレータを使用する前の簡易検討でよく使用します。
ケミカルエンジニアとして精密に計算する能力ももちろん必要ですが、会議の場などでおおまかな値を素早く計算することが求められることがあります。
そのようなときに電卓を叩いてパッと数字を答えられるとイメージアップになりますので、ぜひ覚えてみてください。
おわりに
蒸留のてこの原理について解説しました。
おおまかに蒸留分離後の組成を把握できる手法なので便利です。
